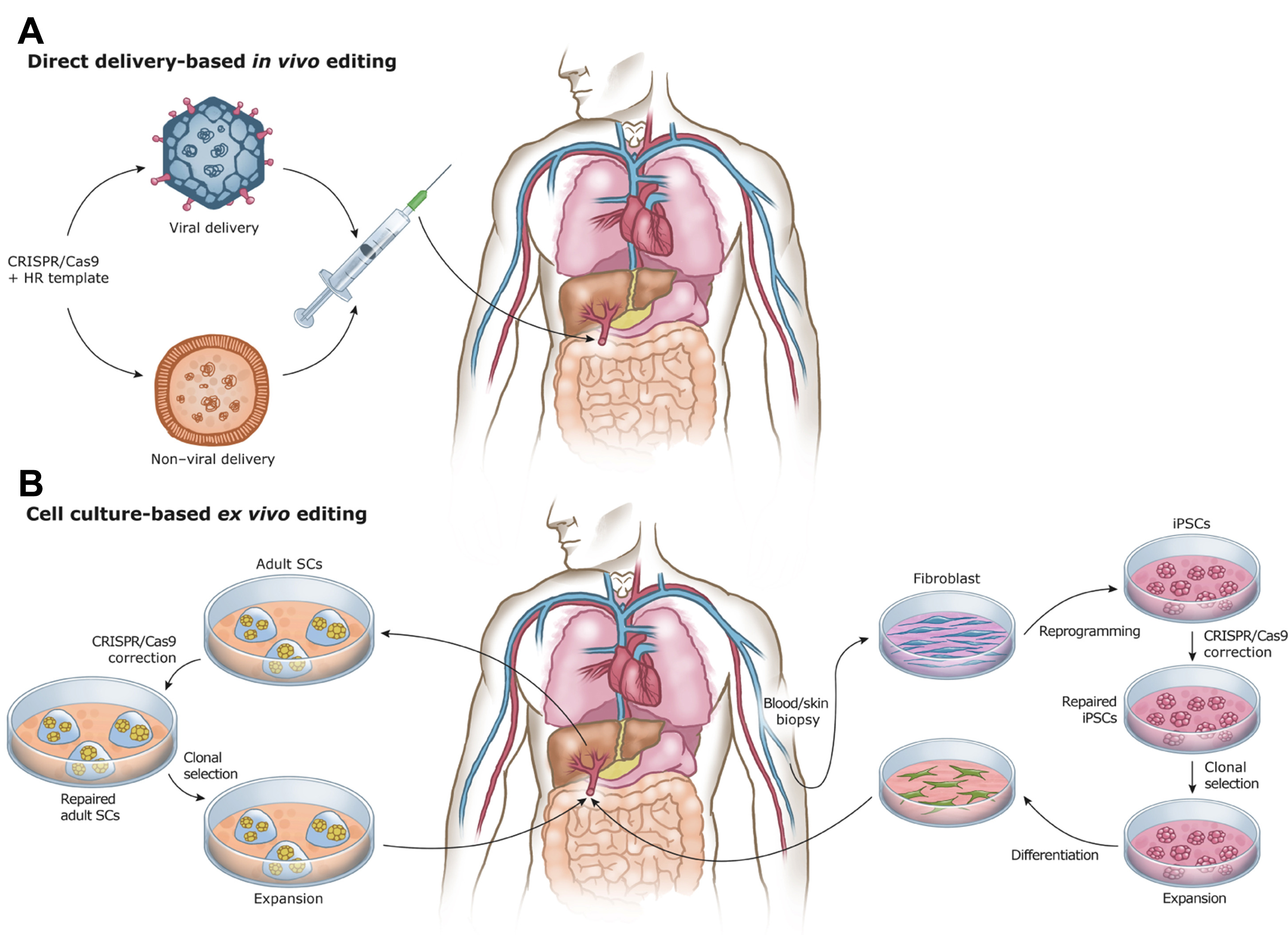
Fig. 1 基因治疗[1][2]


phi29 DNA polymerase具有很强的链置换活性和连续合成的特性,可用于在体外合成双链DNA。
注:在某些应用场景下,使用此酶会有专利限制

TelN Protelomerase可用于合成线性闭合mini DNA载体,其在识别位点 TelRL(56bp)切割双链DNA,并在酶切位点处留下共价封闭的发夹结构,有效地将环状DNA转化为有发夹末端的线性DNA。在实际应用中会将质粒上的目的片段和骨架序列通过TelRL位点间隔。
注:TelRL底物序列需要专利授权
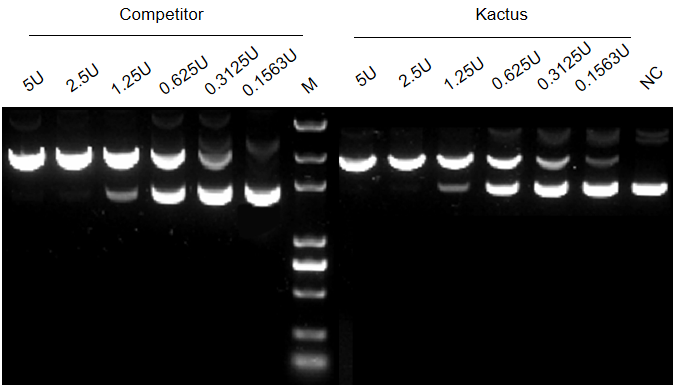
Fig.2 TelN Protelomerase可有效将环状DNA转化为有发夹末端的线性DNA,其活性与知名供应商相当。在50 μl体系中加入513 fmol dsDNA和不同酶量的TelN Protelomerase(由5 U/assay依次2倍梯度稀释,NC为阴性对照),30℃反应30 min。

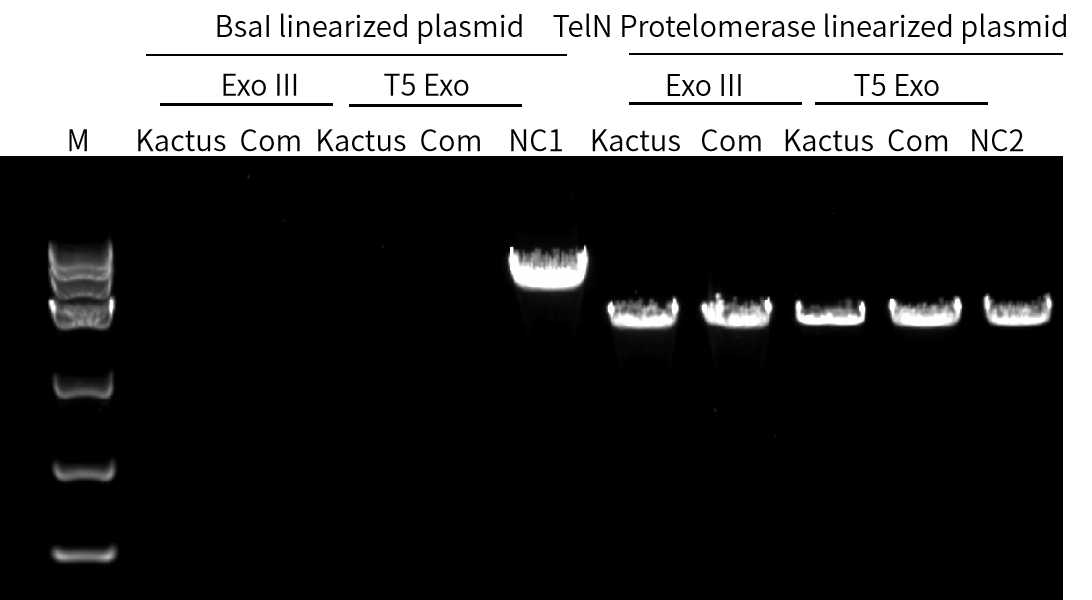
经TelN Protelomerase切割-连接形成的DNA载体有两类,一类含骨架序列,一类含目的片段。骨架序列上有相应的限制性酶切位点,恺佧生物提供高活性的限制性内切酶用于酶切骨架序列。


经TelN Protelomerase切割-连接形成的DNA载体有两类,一类含骨架序列,一类含目的片段。骨架序列上有相应的限制性酶切位点,经酶切后形成平末端或粘性末端,进一步经Exonuclease III作用,达到降解骨架序列,富集目的片段的目的。


主要参与细胞与基因治疗药物(如造血干细胞、T细胞等)的基因修饰, 其中,GMP级Cas9核酸酶于高标准的CGT蛋白酶GMP生产车间生产,并经体外胞内双重验证。已完成DMF备案(编号:036578),并已协助客户完成IND申报;hfCas12Max®是辉大基因(HuidaGene)自主开发的新型DNA基因编辑工具酶,恺佧生物获得在大中华区研究级蛋白的生产销售排他许可,以及GMP级产品的生产销售普通许可。
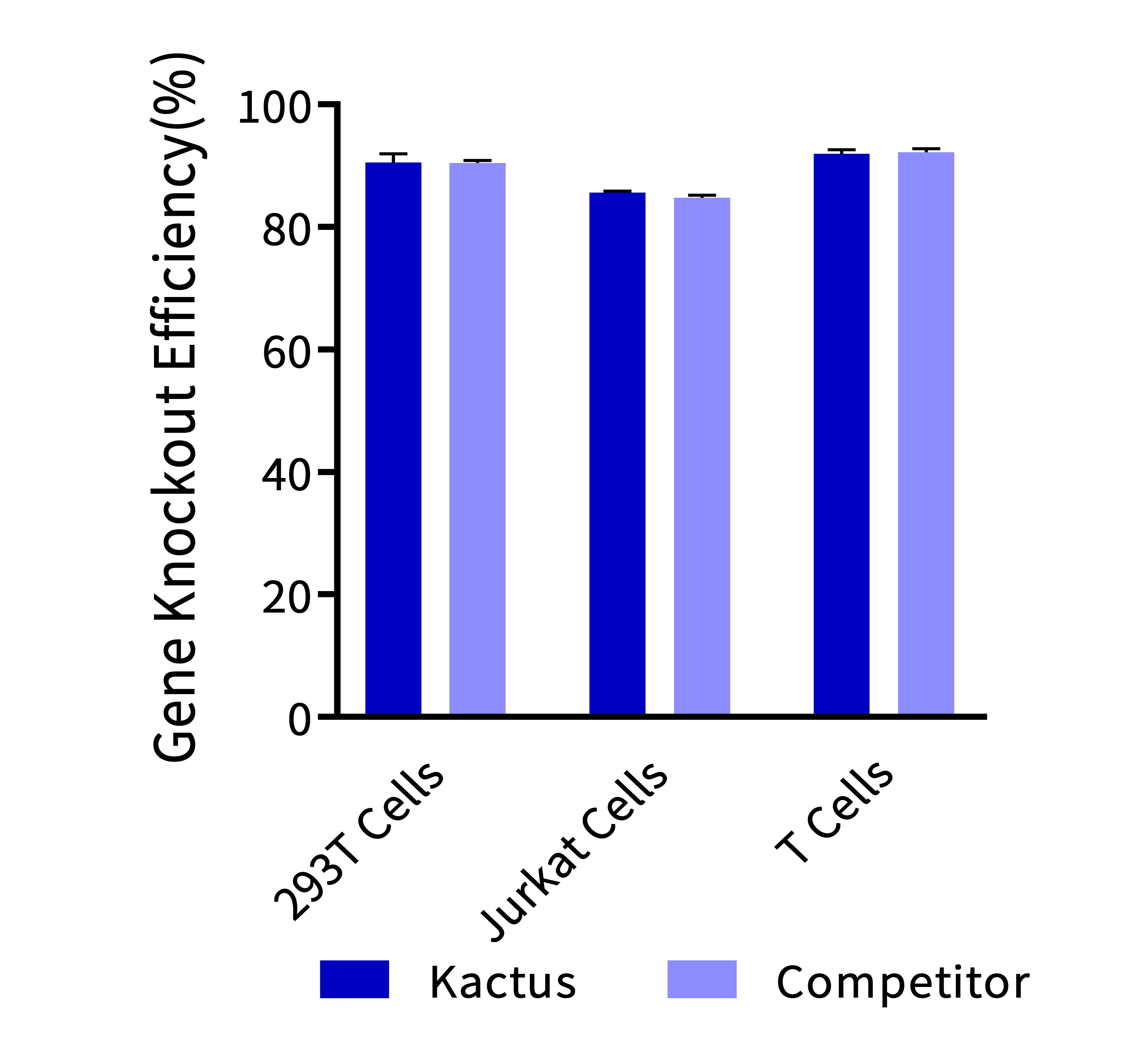
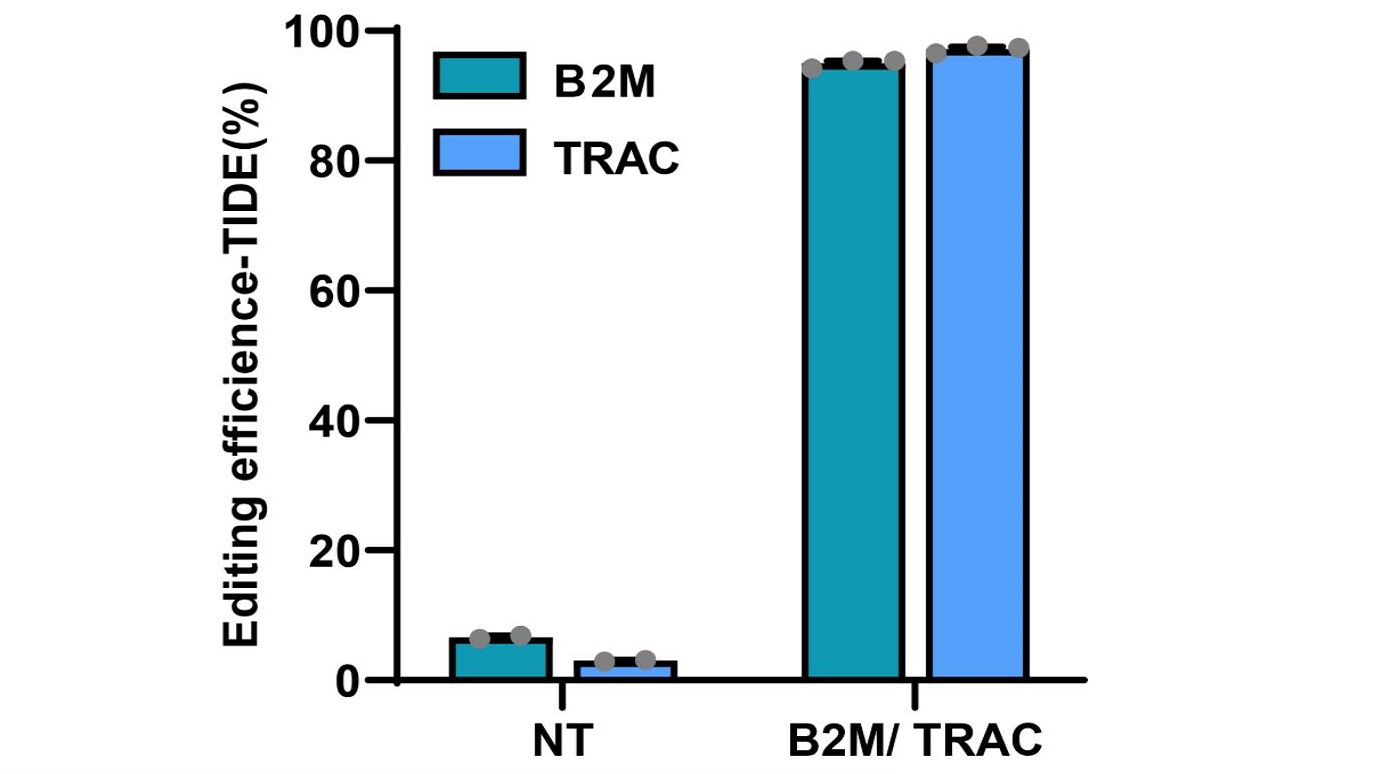


AccuBase®是通过基因工程手段设计的CBE,将窗口范围内的 C 脱氨形成 U,U利用细胞内修复机制转变为 T,从而实现C→T的转变,在编辑的过程中不会引入 DSB,确保了编辑的安全性。此外,创造性地将脱氨酶可逆的包裹起来,只有当 sgRNA 与靶位点结合时才能发挥脱氨作用,大幅度降低了与非靶 DNA 的随机结合,可以实现接近零脱靶的效果,同时维持高效的编辑活性。
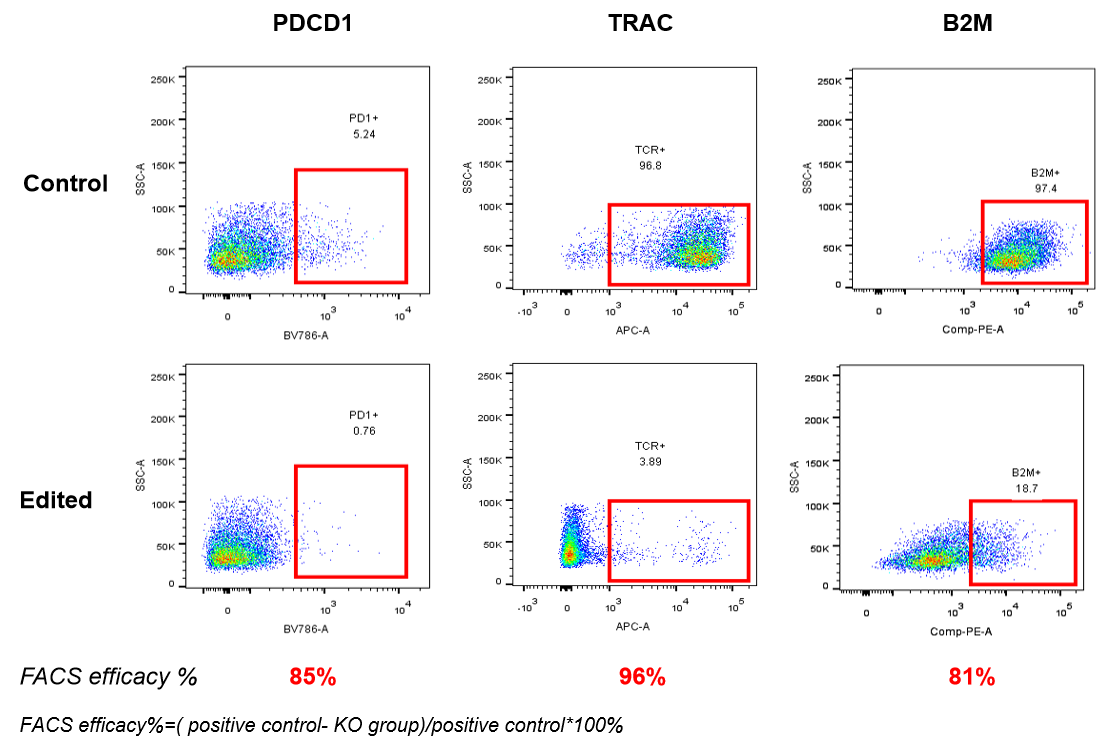
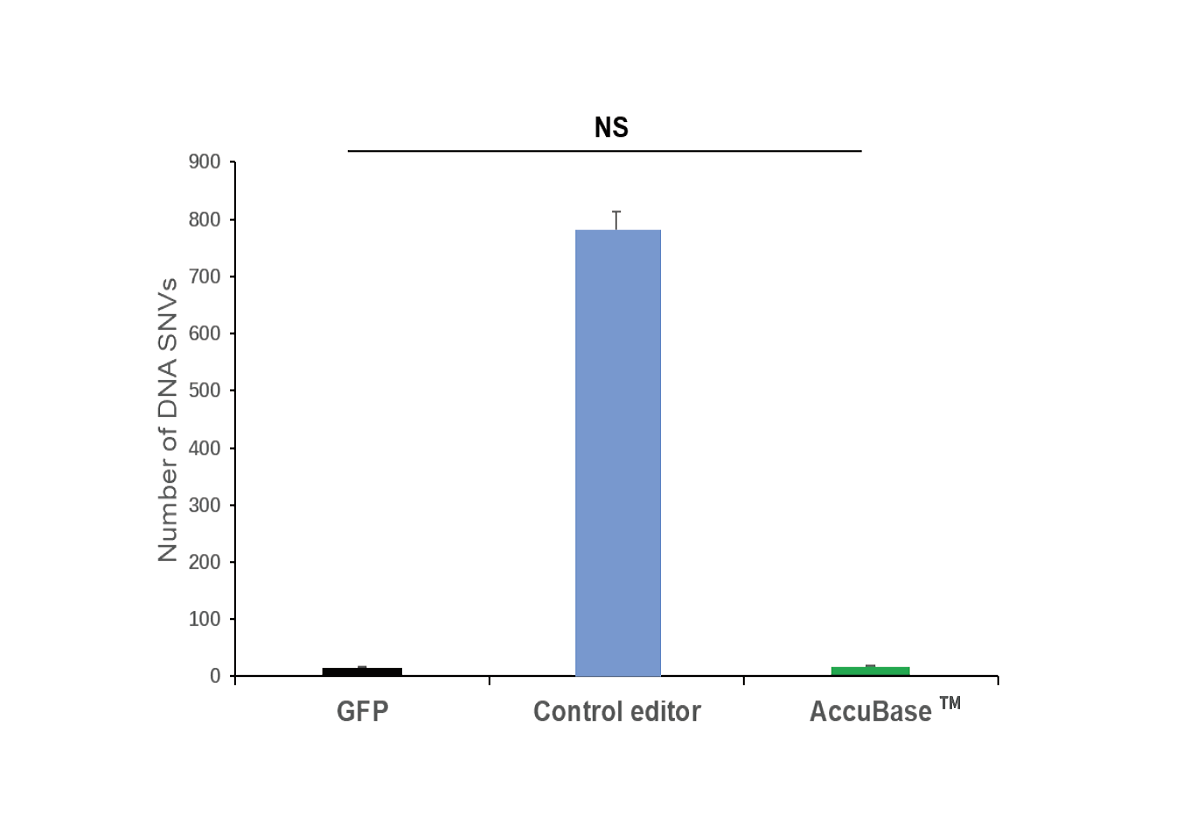

定量检测基因编辑细胞药物在回输人体之前胞外或胞内中Cas9核酸酶的残留。试剂盒检测范围为0.25 ng/ml-16 ng/ml,灵敏度可达0.125 ng/ml。

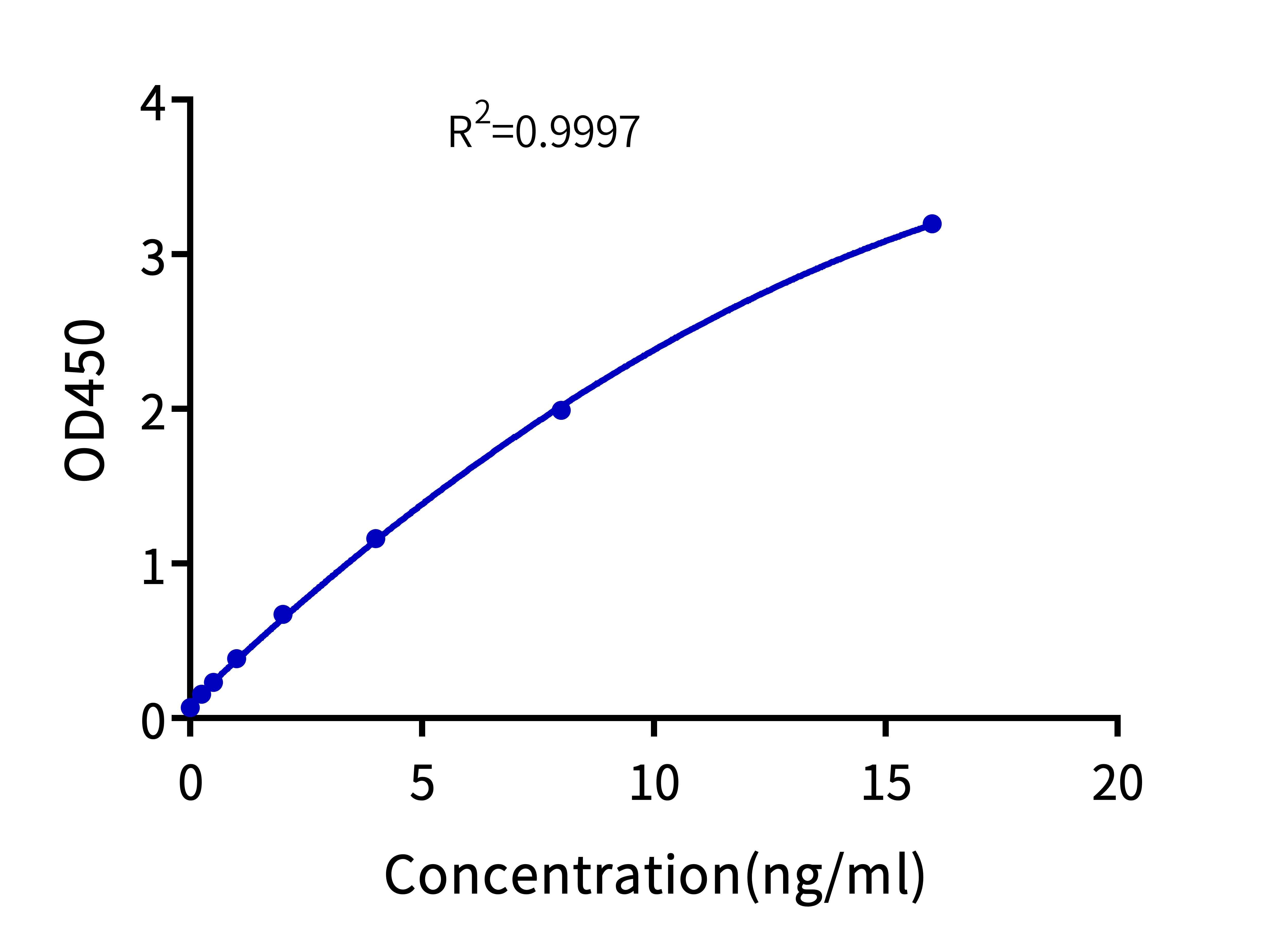

Fig. 10 拟合标准曲线,R2达到0.9997。

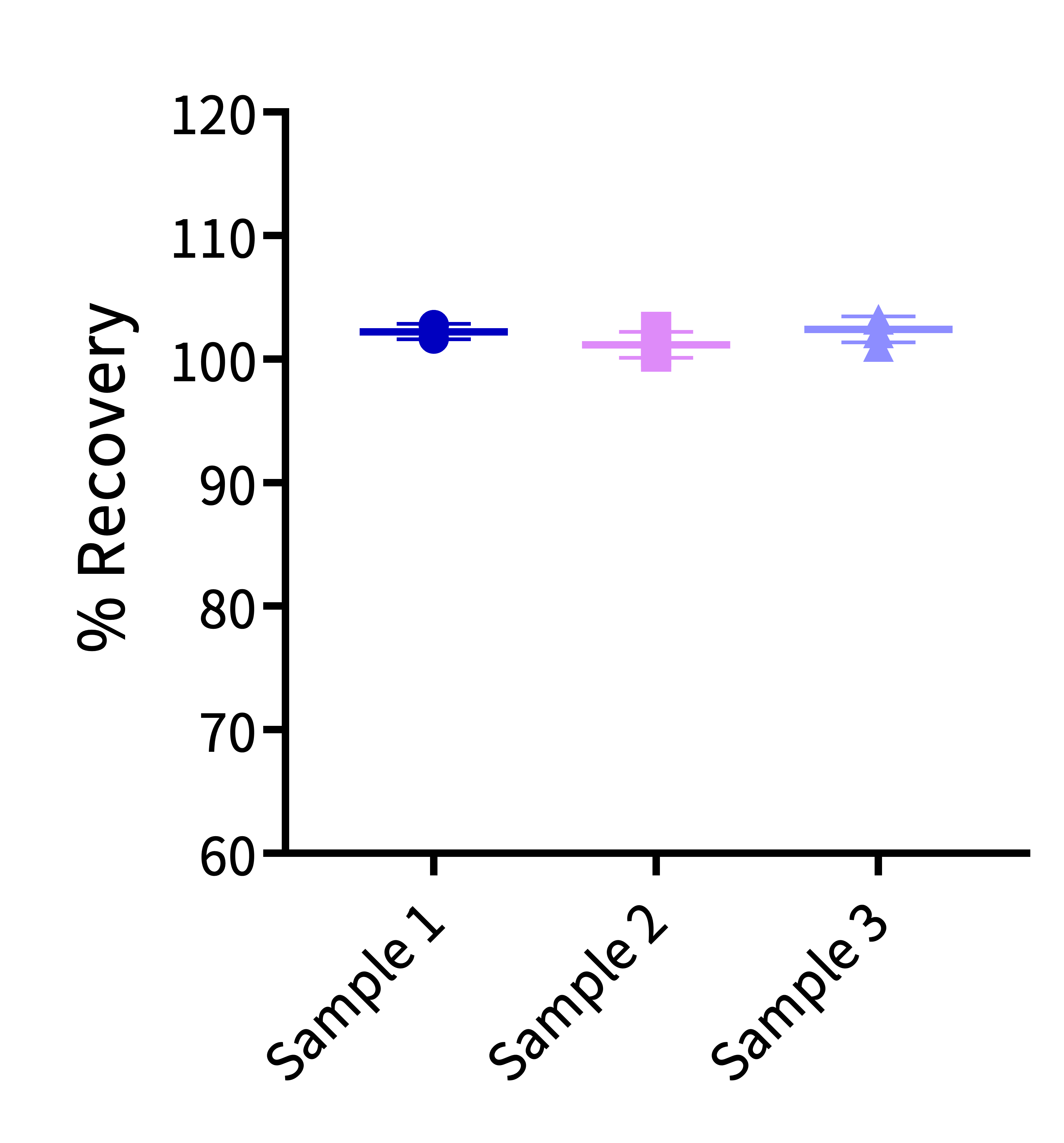

Fig. 11 在稀释缓冲液中检测不同浓度Cas9样本的加样回收率均介于80%-120%,表明本试剂盒检测Cas9核酸酶残留的准确度高。


使用三批次试剂盒分别对高中低三个不同浓度的Cas9核酸酶进行检测,每个样本重复检测10次,计算这10次检测的平均值(M)和标准差(SD),计算变异系数(CV)。
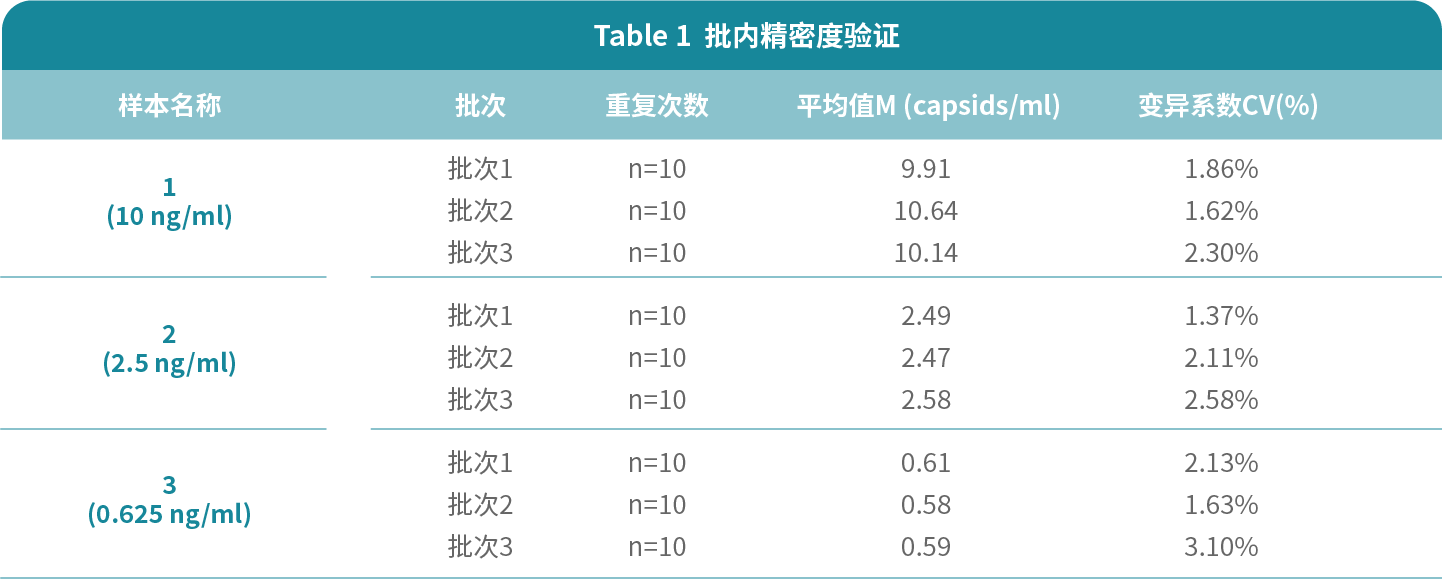
如Table 1所示,每批次试剂盒检测高中低三个不同浓度的Cas9样本的CV均小于10%,表明试剂盒对Cas9的残留检测具有良好的批内重复性。

使用三批次试剂盒对高中低三个不同浓度的Cas9核酸酶进行检测,每个样本使用同批次检测10次,三批次共检测30次,计算这30次检测的平均值(M)和标准差(SD),计算变异系数(CV)。

如Table 2所示,每个样本三个批次间的CV均小于15%,表明试剂盒对Cas9的残留检测具有良好的批间重现性。

AAV是基因治疗领域常用的病毒载体,AAV病毒颗粒滴度的检测方法有Dot blot、TEM、AUC、ELISA、SEC-MALS等。恺佧生物开发了AAV2/5/6/8/9 Titration ELISA Kit,旨在为AAV病毒颗粒滴度的测定提供更便捷、更可靠的解决方案。

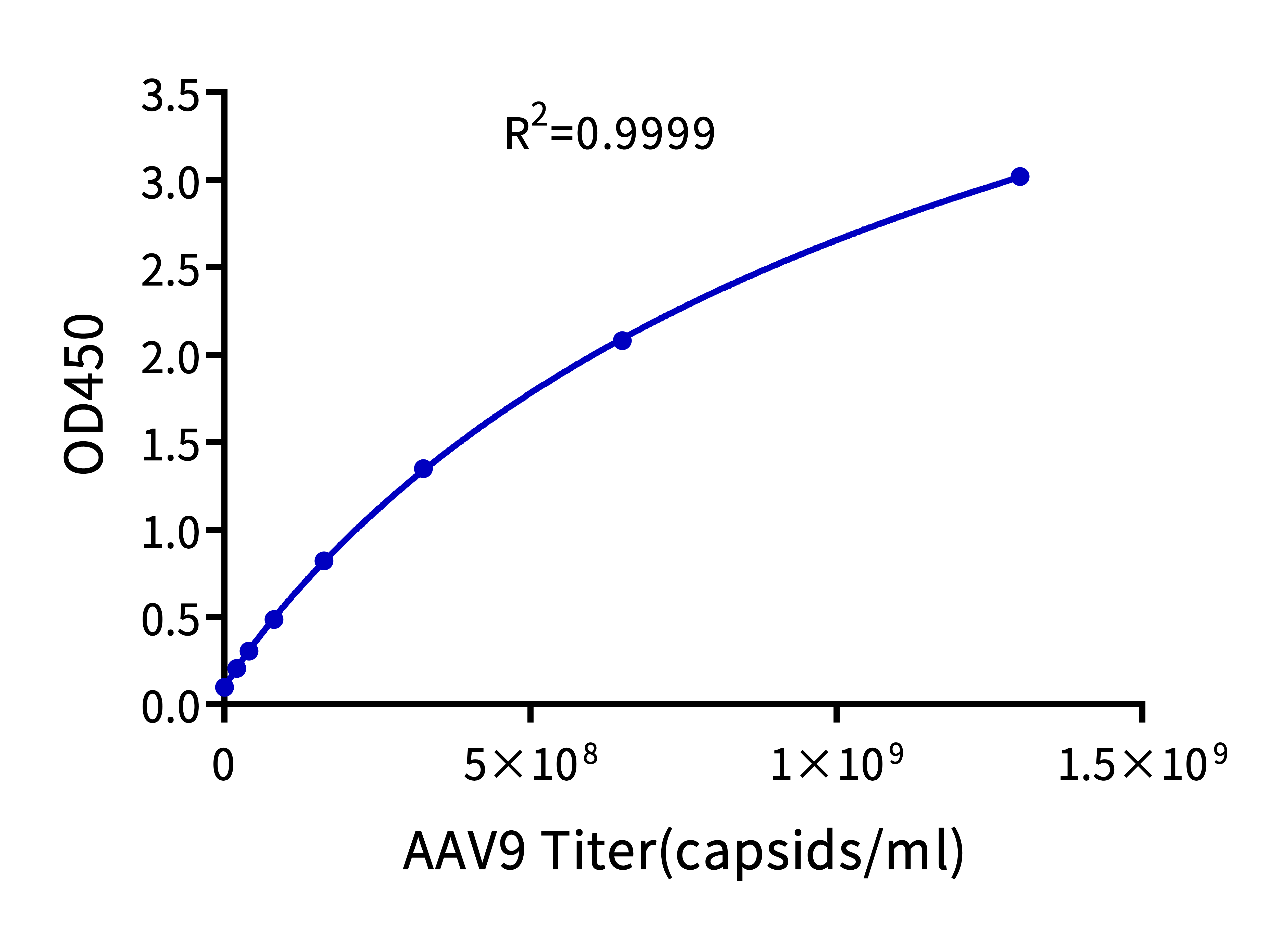

Fig. 12 拟合AAV9 Titration ELISA Kit的标准曲线,其定量范围为2.03E+07-1.30E+09 capsids/ml。

ELISA间接法检测不同浓度的AAV9抗体与AAV2/5/8/9交叉结合,以检测抗体的浓度为横坐标,OD450值为纵坐标绘制曲线;ELISA夹心法检测AAV9抗体与完整AAV9以及变性AAV9的结合,以AAV9的颗粒滴度为横坐标,OD450值为纵坐标绘制曲线。
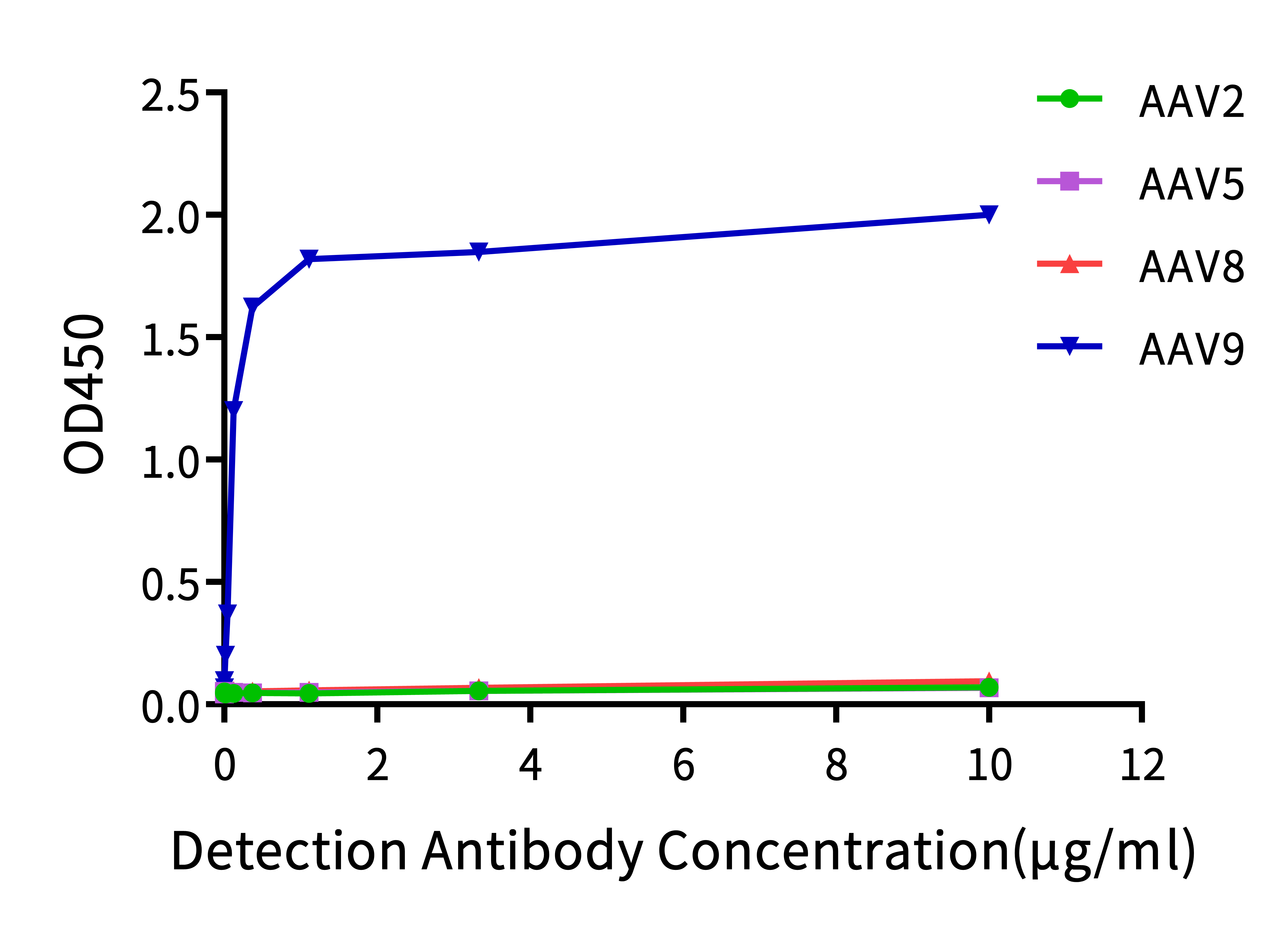
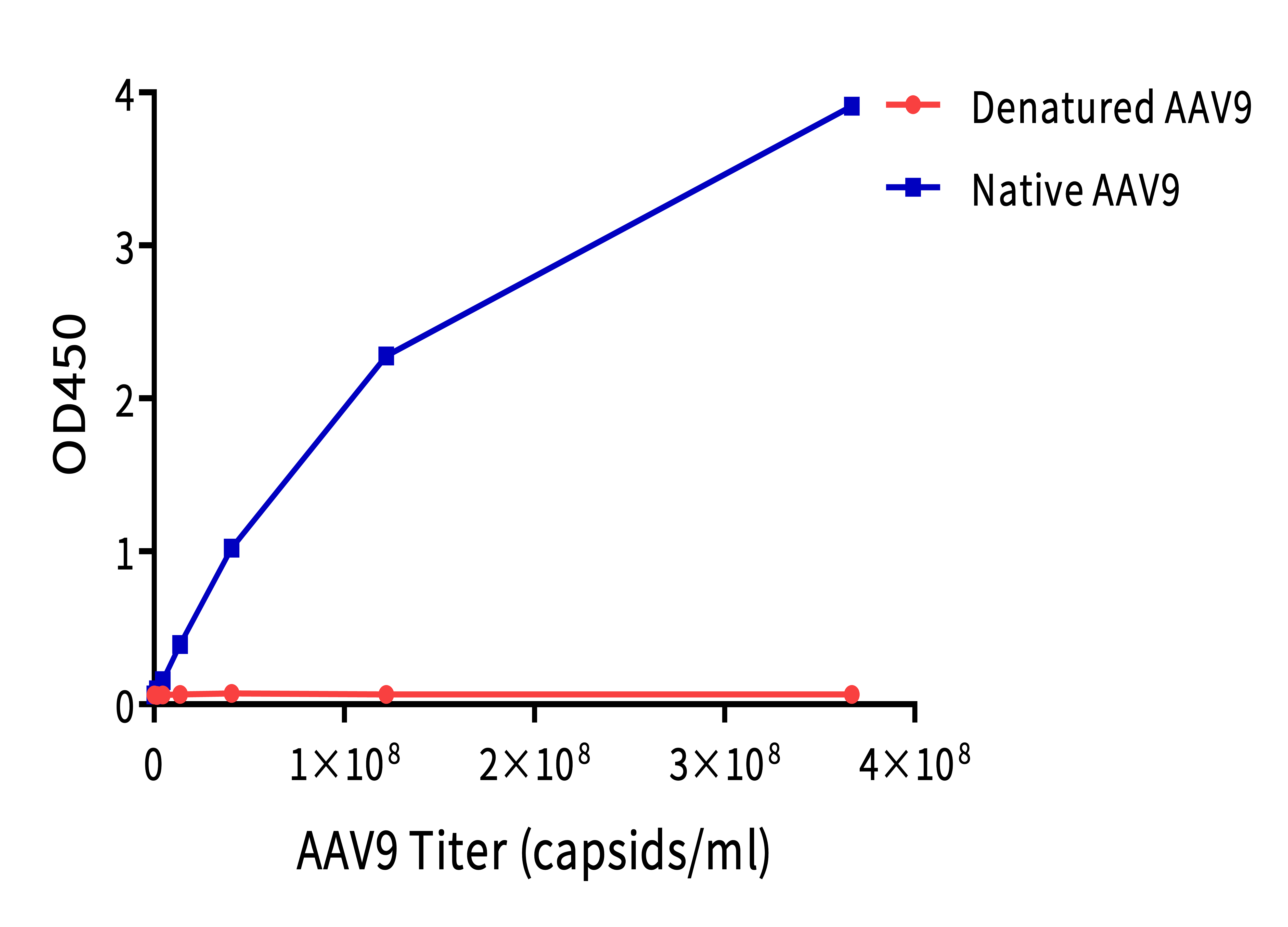

使用同一试剂盒测试高中低三个不同滴度AAV9样本在稀释缓冲液中的加样回收率。
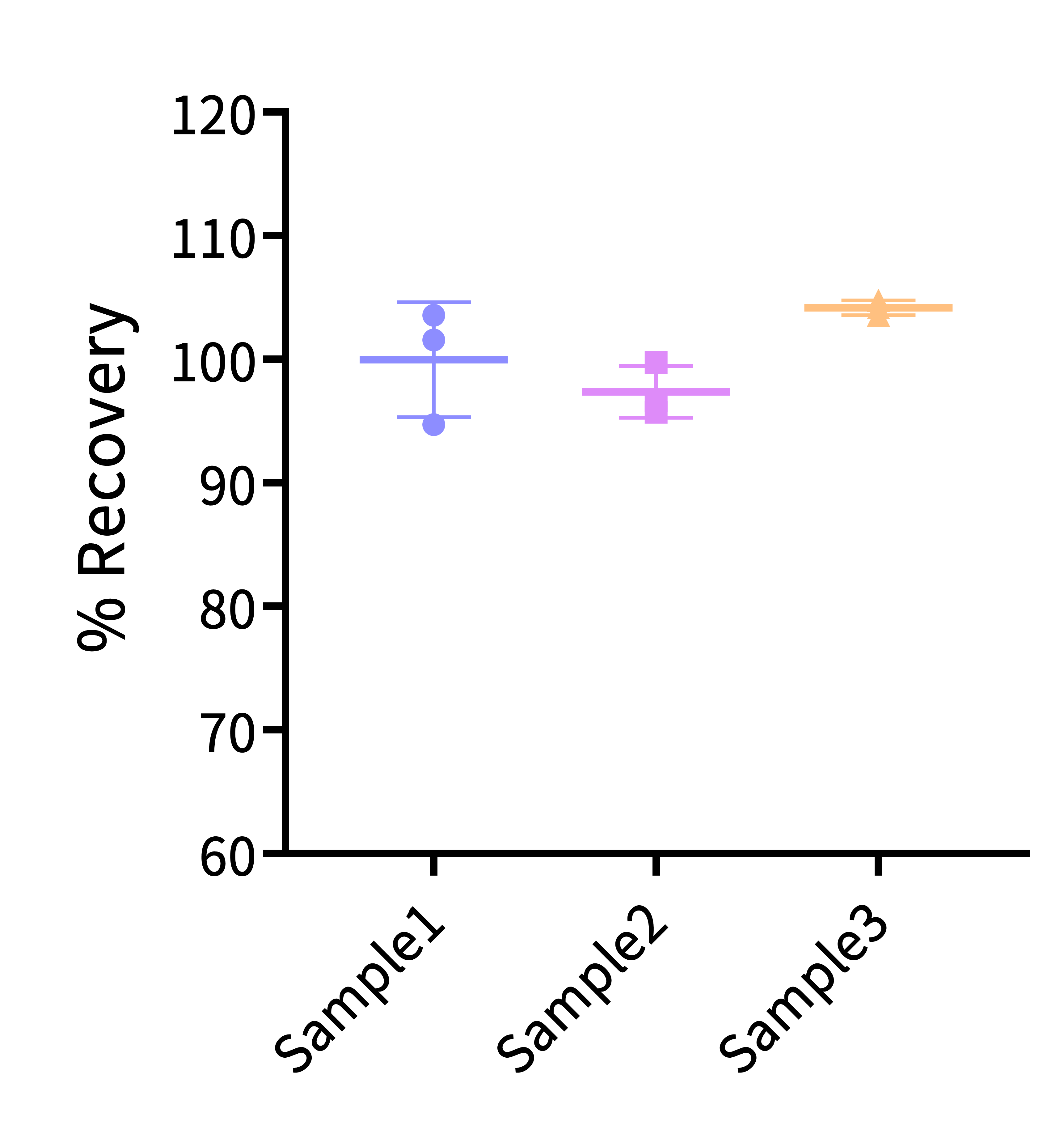

Fig. 15 在稀释缓冲液中检测不同滴度AAV9样本的加样回收率均介于80%-120%,表明本试剂盒检测AAV9滴度的准确度高。

在基因治疗领域,主要用于药物生产过程中去除宿主DNA和质粒DNA等杂质,GMP级MaxNuclease全能核酸酶于高标准的CGT蛋白酶GMP生产车间生产,不使用含动物源原材料,分析方法经系统验证,并经过全方位的QC放行检测,满足从研发到商业大规模生产的使用需求,并且已完成DMF备案(编号:036799)。
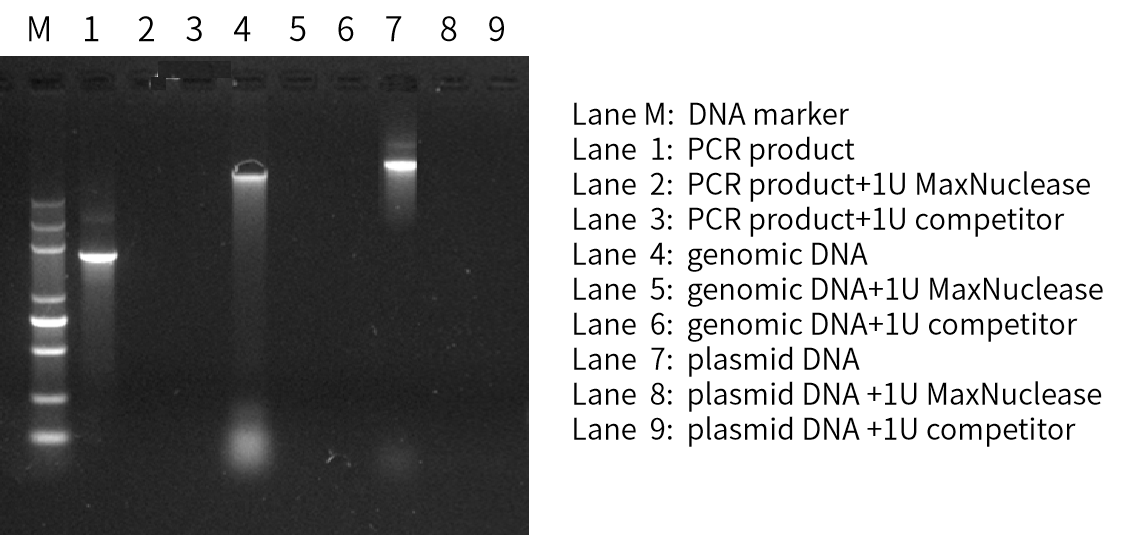
Fig. 16 MaxNuclease降解核酸效果

定量检测基因治疗药物中MaxNuclease全能核酸酶的残留,试剂盒检测范围为46.88 pg/ml-3000 pg/ml,灵敏度可达23.44 pg/ml。
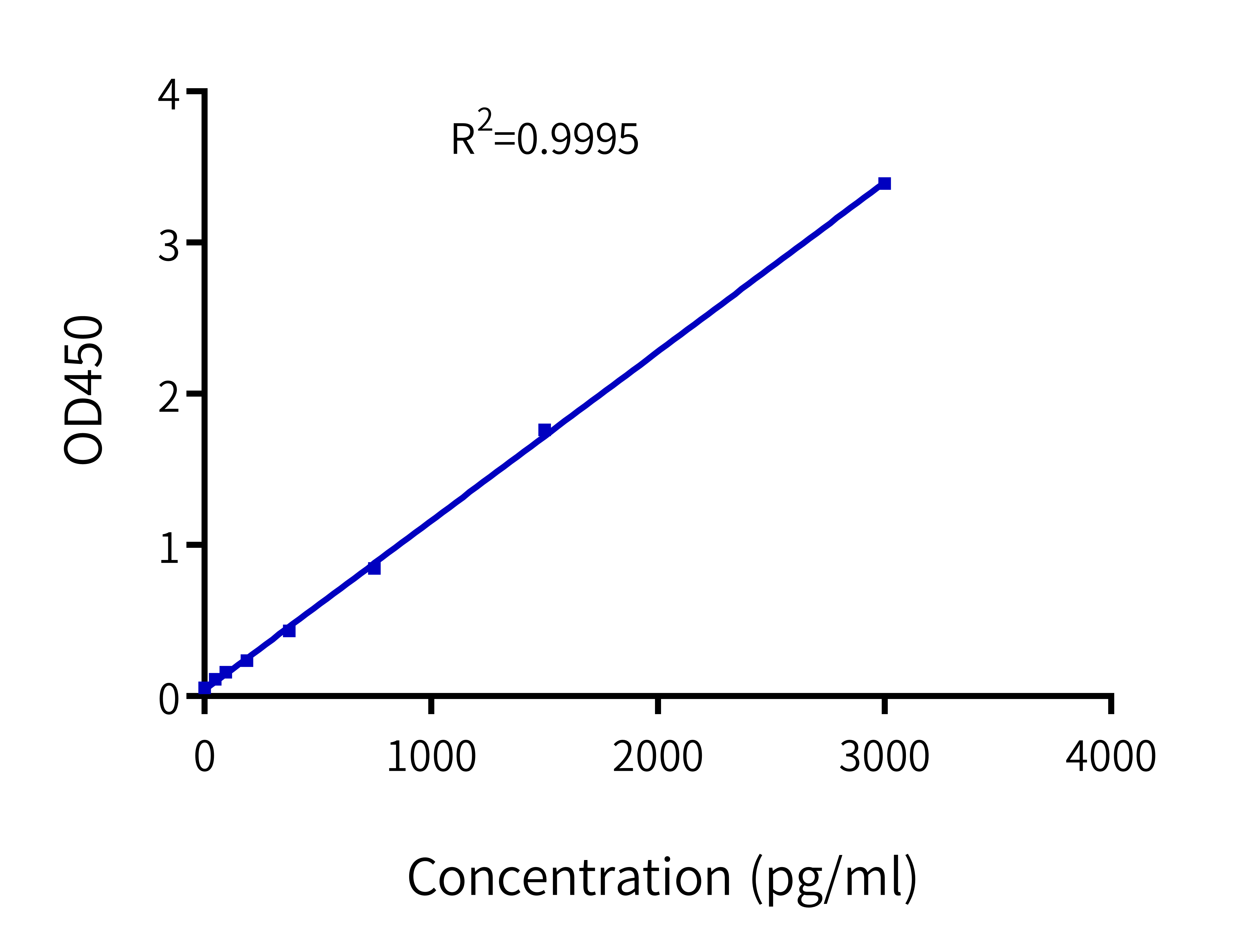

Fig. 17 拟合标准曲线,R2达到0.9995。
| 货号 | 产品名称 | 规格 | |
| PHI-BE101 | phi29 DNA Polymerase | 500 U/5000 U | 立即询价 |
| TLN-BE001 | TelN Protelomerase | 10 kU/50 kU | 立即询价 |
| BSA-EE101 | Bsal | 1000 U/5000 U | 立即询价 |
| GMP-BSA-EE101 | Bsal(GMP grade) | 20 kU/400 kU | 立即询价 |
| BSP-BE101 | BspQl | 1000 U/10 kU | 立即询价 |
| SAP-SE101 | Sapl | 1000 U/10 kU | 立即询价 |
| SAP-SE102 | Sapl V2.0 | 1000 U/10 kU | 立即询价 |
| XBA-EE101 | Xbal | 2000 U/20 kU | 立即询价 |
| EXO-EE101 | Exonuclease III | 500 U/5000 U | 立即询价 |
| KACTUS-CAS9 | Cas9 Nuclease | 1 mg/3 mg | 立即询价 |
| KACTUS-CAS9-GMP | Cas9 Nuclease (GMP grade) | 3 mg | 立即询价 |
| CAS-MM00B | Cas9 (CRISPR Associated Protein 9) ELISA Kit | 96 T | 立即询价 |
| CAS-EE111 | SpCas9 D10A Nickase | 1 mg | 立即询价 |
| CAS-EE121 | AsCas12a Nuclease | 1 mg | 立即询价 |
| CAS-EE128 | hfCas12Max® | 500 μg/1 mg | 立即询价 |
| KD-0001 | BS-EP1(Trade name: AccuBase®) | 200 μg/500 μg/1 mg | 立即询价 |
| GMP-KD-0001 | BS-EP1(Trade name: AccuBase®), GMP grade | 1 mg | 立即询价 |
| AV2-MM00B | AAV2 Titration ELISA Kit | 96 T | 立即询价 |
| AV5-MM00B | AAV5 Titration ELISA Kit | 96 T | 立即询价 |
| AV6-MM00B | AAV6 Titration ELISA Kit | 96 T | 立即询价 |
| AV8-MM00B | AAV8 Titration ELISA Kit | 96 T | 立即询价 |
| AV9-MM00B | AAV9 Titration ELISA Kit | 96 T | 立即询价 |
| NUC-SE101 | MaxNuclease全能核酸酶 | 50 kU/250 kU/5 MU | 立即询价 |
| GMP-NUC-SE101 | MaxNuclease全能核酸酶(GMP grade) | 250 kU/5 MU | 立即询价 |
| NUC-SE00B | MaxNuclease ELISA Kit | 96 T | 立即询价 |

[1] 体内基因治疗产品药学研究与评价技术指导原则(试行)
[2] Savić N, Schwank G. Advances in therapeutic CRISPR/Cas9 genome editing. Transl Res.






